Una pareja gallega con antecedentes de ceguera congénita en su familia y un primer hijo con el Síndrome de Norrie, una rara enfermedad hereditaria recesiva que causa ceguera congénita y otras secuelas, han tenido una niña libre del síndrome gracias al diagnóstico preimplantacional. Esta técnica consiste en estudiar los embriones antes de implantarlos en el útero materno. En este caso, todos los embriones resultaron ser femeninos, pero el nacimiento de la niña sana se ha logrado, por primera vez en el mundo, sin recurrir a la selección de sexos, de modo que se abre la puerta a la posibilidad de tener varones sanos y no portadores de la enfermedad. Lo explica Elkin Muñoz, director de IVI Vigo, y autor del caso junto a Julio Martín, director del laboratorio de Diagnóstico Genético Preimplantacional para enfermedades monogénicas del IVI Valencia.
Una enfermedad monogénica, es decir, que afecta a un solo gen ubicado en el cromosoma X. Consiste en un defecto en la retina por el cual no se transmite correctamente la información neurológica, de modo que los niños nacen ciegos. La ceguera es congénita. También puede afectar al oído, aunque la sordera se presenta más tardíamente y, en algunos casos, sufrir retraso mental.
En España no está cuantificado, pero es una enfermedad rara que afecta a muy poca población.
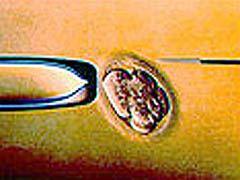
El diagnóstico preimplantacional es un estudio que se realiza sobre los embriones antes de que éstos sean implantados en el útero de la madre. Primero realizamos el tratamiento de fecundación in vitro (FIV) convencional: estimulamos los ovarios de la mujer con una técnica muy sencilla que se efectúa en muchos centros en España. Después los ponemos en contacto con los espermatozoides de la pareja y obtenemos los embriones.
En su tercer día de vida, le extraemos al embrión una o dos células y analizamos si tienen o no la mutación que hace que aparezca la enfermedad. Nosotros lo que hemos hecho por primera vez con esta técnica es obtener embriones libres de esta enfermedad sin selección de sexo.
Antes, en esta enfermedad, se hacía una selección de sexo igual que sucede con la hemofilia. Se transmite por las mujeres, pero sólo la padecen los hombres. Hasta el desarrollo de esta técnica de diagnóstico preimplantacional se hacía una selección de embriones femeninos sin saber si estaban afectos o sanos. En este caso, hemos buscado transferir los embriones no portadores, masculinos o femeninos, libres de la enfermedad. De la otra forma, si se selecciona el sexo, las niñas estarían en la misma situación de la madre: serían portadoras de la enfermedad y la tendría su futuro hijo nacido con la mutación. En cambio, con nuestra técnica hemos conseguido cortar la transmisión de la enfermedad de Norrie en esa familia.
Una vez efectuado el análisis de las células, ya sabemos cuáles son las enfermas y cuáles son las sanas. Para tranquilidad de la población, cabe decir que no implantamos 500 embriones -una gran cantidad-, sino 3, 4 o 5 como mucho. En este caso, la pareja que vino a nuestra consulta ya tenía un hijo varón afectado y había recibido dos ciclos de FIV.
«Queremos crear líneas celulares para estudiar el comportamiento de las células enfermas y poder probar nuevos tratamientos»
En la primera fecundación in vitro se le transfirieron los embriones de dos varones sin la enfermedad, pero la paciente no se quedó embarazada. Y, en la segunda, se le transfirieron los embriones de dos niñas, una libre de la enfermedad y otra portadora. No teníamos más embriones; todos los demás estaban afectos. En este segundo ciclo, se quedó embarazada de la niña sana.
No existe tratamiento para esta enfermedad, al igual que ocurre con todas las enfermedades monogénicas. Lo que hay es terapia de apoyo para tratar las consecuencias o secuelas de la enfermedad, pero no para su curación.
Correcto. Nosotros también tenemos experiencia así como otros centros a nivel mundial, para aplicarlo a otras enfermedades. En concreto, lo hemos realizado en dos nuevas (aparte de la hemofilia, la talasemia o la distrofia muscular de Duchenne): la linfohistiocitosis hemofagocítica el año pasado y, en este caso, la enfermedad de Norrie, también logrado en exclusiva por IVI Vigo, ya que antes nunca se había conseguido.
Tenemos diferentes formatos de investigación abiertos. Relativos al laboratorio de diagnóstico preimplantacional, estudiamos su aplicación en más enfermedades monogénicas. Aunque en realidad hay más de 20.000, tenemos 200 perfectamente tipificadas y en el IVI hemos trabajado sobre 40. Éste es un campo muy amplio. Dentro de este mismo laboratorio, también estamos trabajando en una aplicación técnica con beneficios a terceros, que es el «bebé medicamento».
Consiste en formar embriones y seleccionar aquellos inmunológicamente similares o compatibles con un hermano enfermo para obtener las células del cordón umbilical cuando nazca, a fin de poder tratar a su hermano de enfermedades hematológicas como la leucemia o la anemia de Fanconi.
Lo estamos empezando a hacer. Aún no se ha desarrollado en España. La Comisión Nacional de Reproducción Asistida nos ha autorizado a tratar a tres familias, pero aún estamos en ello.
El IVI tiene muchos embriones enfermos y lo que nos planteamos es, a medio plazo, crear líneas celulares para estudiar el comportamiento de las células enfermas para, en el futuro, poder probar los tratamientos de estas enfermedades sobre esas líneas celulares. Ésta es una de las posibilidades de desarrollo a medio plazo.
Correcto, si quieres evitar la aparición de la enfermedad es la línea en la que hay que trabajar, puesto que a la terapia génica le faltan muchos años; no es algo que ya esté y que ya tenga aplicación. Y lo mismo ocurre con las células madre.
El diagnóstico preimplantacional (DPI) comenzó a realizarse hace unos seis años y, aunque ha sido una apuesta de la sanidad privada, también hay muchos centros públicos trabajando en él. Gracias a esta innovadora técnica que resuelve los problemas de reproducción de las parejas afectadas por enfermedades hereditarias, el IVI ha conseguido 65 gestaciones y nacimientos de niños sanos libres de enfermedades hereditarias. La lista de enfermedades monogénicas candidatas a la realización del diagnóstico genético preimplantacional es amplia.
Entre ellas figuran las ligadas al cromosoma X, como el Síndrome del X frágil, la distrofia muscular de Duchenne y Becker, la hemofilia A, la atrofia muscular bulboespinal (enfermedad de Kennedy, la incontinencia pigmenti, el síndrome de Alport, el déficit de omitina transcarbamilasa y la propia enfermedad de Norrie). Pero también habría otra amplia lista de enfermedades de herencia autosómica recesiva y de herencia autosómica dominante que se pueden detectar en los embriones de los padres afectados y, por lo tanto, evitar, que los niños que nazcan las padezcan, gracias al DPI.